第25回日本医学会総会
「医療における電解機能水」(アルカリイオン水、アルカリ還元水)
日時:平成11年4月2日(金)
場所:東京ビックサイト
アルカリイオン水(還元水・水素水)の効用の検証
北洞 哲治(国立大蔵病院 消化器科)
緒言
”医療と水”、これは古くより重要な関わりをもってきたが改めてとりあげられることは少なかった。水は、いろいろな面で医療と関わってきたがここでは飲用水の面より考えてみたい。かつて飲用水の多くは川水あるいは地下水を用いていた。飲用水は水量が豊富であり、安価であることが第一であり、その条件を満たしていた。しかしながら、川水、地下水は汚染されやすい状態にあり、飲水を介した経口伝染病が時として問題となった。そのため川水を消毒し安全性を高め、伝染病を予防する目的で上水道が整備され、多くの経口感染症の予防が達せられ、水道水は豊富で、安価でかつ安全であることより飲用水としての地位を認知されるところとなった。
近年、水の生体に与える影響が様々な分野で論議される中、飲用水においても豊富、安価、安全の3条件のみならず、おいしい水であること、体に良い(無害)水であることのより積極的な条件が付加価値として求められるようになった。その中で水道水から容易に生成され、健康との関わりも示唆されているアルカリイオン水(還元水・水素水)(電解機能水、アルカリイオン水(還元水・水素水)、アルカリ還元水)が注目の対象となりつつある。
わが国で開発された独自のアルカリイオン水(還元水・水素水)は、種々の腹部愁訴に対する効能を有する唯一の飲用水であり、健康の維持・増進、そして疾病の予防・改善にもその効用が期待されている。アルカリイオン水(還元水・水素水)の効用の優れた傍証はこれまでいくつかなされてきたが、その時代的背景もあり、それらは今日的論拠には不充分であるとする気運が高まり、アルカリイオン水(還元水・水素水)効用に対する信憑性への疑問とともに今日的科学的検証が要望されるに至った。
これらの背景をもとに、平成5年アルカリイオン水(還元水・水素水)整水器委員会が組織され、アルカリイオン水(還元水・水素水)の生体に与える影響につき検証が試みられてきた。本内容はそこで検討されたもので、第一にアルカリイオン水(還元水・水素水)の臨床的検証、第二にアルカリイオン水(還元水・水素水)の物性の解析、第3にアルカリイオン水(還元水・水素水)の生体に与える影響の基礎的検証の三本柱よりなっている。各研究ともそれぞれ顕著な成果がみられつつあり、今後、医療の分野で電解機能水がどのような役割を果たしていくのか期待されるところである。ここでは、研究の現状を紹介とするが、電解機能水の有効性を展望する中、さらなる研究の発展が望まれるところである。
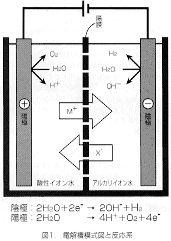
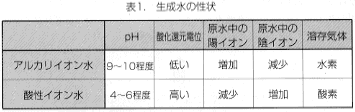
| アルカリイオン水(還元水・水素水)とは アルカリイオン水(還元水・水素水)は、水にカルシウム剤を添加し、電気分解することにより得られるアルカリ性の水の呼称である。アルカリイオン整水器は、水道に直結した水道水より流水下に電気分解する流通式(フロー式)と、毎回一定量の水道水を入れて滞水下で電気分解する貯槽式(バッチ式)の2種類に大別されるが、いずれの場合も電解槽の構造および電気分解の原理は同じである。 電解槽は図1のように隔膜により2つに分けられており、それぞれに陽極および陰極となる電極が設けられている。隔膜は水中のイオン種を自由に通過させ、水そのものの自由な通過を阻害する。流通式ではこの電解槽に水の流入口と流出口が設けられており、水が両極間を通過する。この電解槽にカルシウムイオンを含む水を入れ、両電極を通して水に直流電流(実際の商品では家庭用の交流電流を直流に整流する)を流すと、塩化物イオン、炭酸イオン、硫酸イオン等の陰イオン(X-)は陽極に引き寄せられ、カルシウムイオン、マグネシウムイオン、ナトリウムイオン等の陽イオン(M+)は陰極に引き寄せられる。両極間にかかる電圧が十分に大きければ、電極の表面において水が電気分解され陰極側では水酸化イオン(OH-)、陽イオンおよび溶存水素が多くなり、phの高いアルカリイオン水(還元水・水素水)が生成される。アルカリイオン水(還元水・水素水)の性状は表1のごとく表される。 |
  |
アルカリイオン水(還元水・水素水)の性質と安全性
水道水またはそれにカルシウム塩を添加した“水”をカソード(陰極)で電気分解して得られるアルカリイオン水(還元水・水素水)を製造する装置であるアルカリイオン整水器は今日では主として流通方式(フロー式)の装置が市販され、非常に使いやすくなっている。この整水器にもいろいろな材料が使われるようになっている。そこで、整水器から溶出する物質と、整水器中で生成する可能性のあるトリハロメタン類を中心に安全性について物性を中心に調べた。
1.安全性
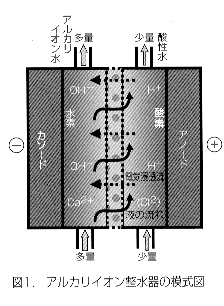
市販されているフロー式のアルカリイオン整水器の大多数は図1に示す構造をしている。水を電気分解してアルカリ性の水を得るのであるからカソードで還元反応が進行して水素が発生してアルカリ性になるとともに、アノード(陽極)では水が酸化されて酸素が発生して酸性水が生成する。アルカリ水と酸性水が混ざって中性水になることを防ぐために隔膜が間に設けられている。この際、塩化物イオンが含まれるとこれが酸性水側で酸化を受けて塩素となる。フロー式の整水器の多くは、機器のメンテナンスと清浄化のために、時々電源からのつなぎ方を変えて極性を反転させて、本来ならカソードとして働く電極をアノードに、アノードをカソードになるようにして短時間電気分解をする。この逆通電の影響についても調べてみた。
整水器の材料
白金被覆チタン電極と一部で使われているフェライト系の電極を試験の対象とした。これらの電極を備えた図1の試験用モデル装置を作成し、アルカリイオン水(還元水・水素水)を分析した。白金被覆チタン電極では重金属などの溶出の問題は認められなかった。フェライト電極を用いた場合にも、アルカリイオン水(還元水・水素水)生成時には重金属の溶出は問題とならない。しかし、洗浄のための逆通電時には微量の重金属の溶出が見られる。逆通電後に通水だけを行うことによってこの溶出した重金属は洗い流され、正規運転時には問題とならない。なお安全を期するために白金被覆チタン電極などへ転換することが望ましい。
電極の試験に加えて、電極以外の配管チューブ、ガスケット材、ハウジング材などの主なものについてアルカリイオン水(還元水・水素水)への浸漬試験を行ったが、問題となる物質の溶出は見られなかった。
アルカリイオン水(還元水・水素水)中の副生成物
アルカリイオン水(還元水・水素水)整水器に導入される水に塩化物イオンが含まれると、これがアノードで酸化されて塩素が生成し、水に含まれる微量有機物などと反応して有機塩素化合物を生成することが懸念される。とくに、塩基性の条件の下でハロホルム反応によってトリハロメタンなどが生成する可能性がある。
整水器の普通の状況ではハロホルム反応は進行しないが、隔膜を通って塩素を含む酸性水がアルカリ水側に移動してくると、ハロホルム反応の条件が出現してトリハロメタン類が生成することがある。図1の試験装置を工夫して酸性水側からアルカリ水側に流れを起こして調べたところ、トリハロメタン類が有害とされる濃度を越して上昇した。電気分解をすると使用する隔膜の特性によっては電気浸透が起こって酸性水がアルカリ水側に移動することがある。しかし、実際のアルカリイオン整水器を数種類調べた結果、電気浸透流の大きい装置はなく、また、電解部分への水の流入と電解水の流出を工夫してアルカリ水側から酸性水側へ流れが生じるように工夫されており、ハロホルム反応の条件にはならず、トリハロメタン類の生成は認められなかった。
なお、製品をより安全にするために、工業会に報告し、製品安全基準の刷新を行わせた。
2.アルカリイオン水(還元水・水素水)の性質
アルカリイオン水(還元水・水素水)の性質については電気分解の化学からはまったく新規である説がいくつか提出されているが、試験結果では、従来の電気分解の学問の枠を超える性質は認められなかった。すなわち、電気分解によってカソード側であるので水素が発生し、それに伴ってカソード付近の水がアルカリ性になる。
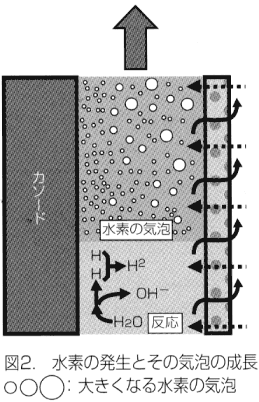
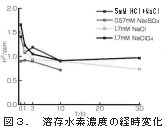
| アルカリイオン水(還元水・水素水)のph 水の電気分解によって次のように水素が発生してOH-が生成してカソード近傍ではアルカリ性になる。電気的中性を保つためにCa+のようなカチオンが移動してくるとともに、OH-が酸性水側に移動していく。又、酸性水側からH+が移動してくる。これらの物質移動のバランスによってアルカリイオン水(還元水・水素水)のPHが決まる。電解電流を大きくしてOH-の生成速度を速くし、液の流れを遅くすればphが高くなる。 水の電気分解によってカソードから水素が発生するが、この水素は最初極めて微小な気泡となっている。図2に示すように、これが溶液中で他の小さな気泡を集めて大きな気泡に成長する。カソードで水素原子が水素分子になり、溶液中に溶けた水素分子が集まって微小な気泡になるが、この気泡になるためには余分なエネルギーが必要であって、電極の近傍では平衡溶解度より高濃度で水素が溶解している。例えば、水素ガスの直径が100nmの場合、その気泡のガス圧は30気圧となって、周りの水素の溶解度も30気圧と平衡にある。水素の過飽和度については100を越すような大きい値も報告されている。このようなわけで、アルカリイオン水(還元水・水素水)中には水素の溶解度が高いと考えられる。水素の溶解度はアルカリイオン水(還元水・水素水)の“酸化還元電位”を低くして還元性雰囲気を作り出す。したがって、アルカリイオン水(還元水・水素水)中の水素の溶解度はその性質に影響する。 水素の溶解度を測定するのは容易ではなく、又、過飽和であってもそれは徐々に低くなる。いくつかの塩を含む水から作ったアルカリイオン水(還元水・水素水)を2度Cで放置したときの水素の濃度を図3に示す。2日目で急速に低下するが、長期間高濃度で保たれる。 |
   |



